Harika bir konu seçimi! Madde ve Endüstri ünitesinin en keyifli kısımlarından biri olan Asitler ve Bazlar konusuna hemen göz atalım. Gönderdiğin görseldeki bilgileri ve etkinliği senin için adım adım analiz edip açıklayacağım.
Soru 1: Görseldeki Tablo 4.2’de yer alan asit ve bazların günlük hayattaki isimleri ve kullanım alanları nelerdir?
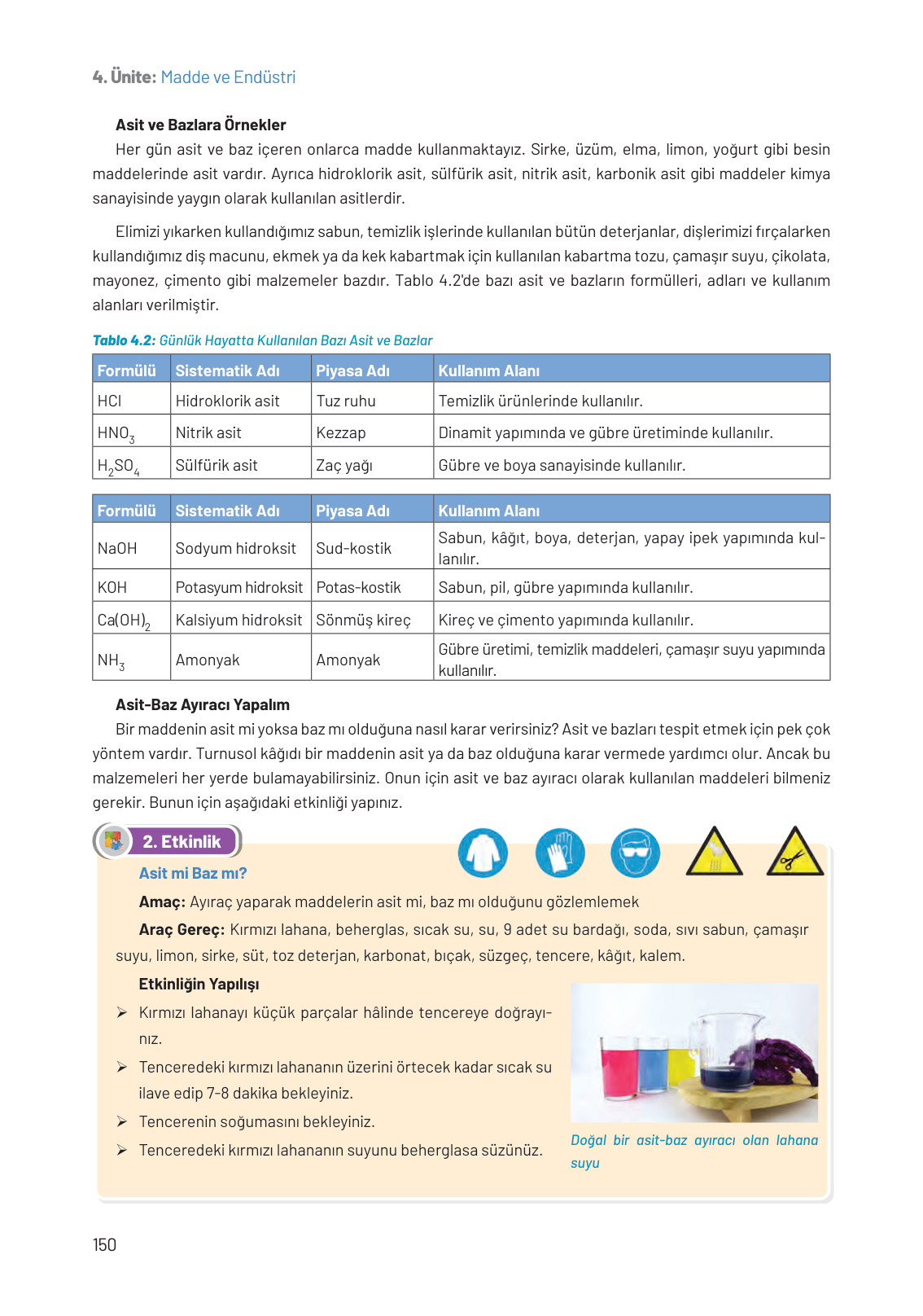
Sevgili öğrencim, bu tablo aslında kimya dersinde gördüğümüz formüllerin ve bilimsel isimlerin günlük hayatta nerelerde karşımıza çıktığını gösteren çok güzel bir özet. Birlikte inceleyelim.
Unutma, asitlerin ve bazların birçoğu tehlikeli olabilir, bu yüzden onlarla çalışırken çok dikkatli olmalıyız.
Çözüm:
Tabloyu iki kısma ayırarak inceleyelim: Asitler ve Bazlar.
ASİTLER
- Formülü: HCl
- Sistematik Adı: Hidroklorik asit
- Piyasa Adı:Tuz ruhu
- Kullanım Alanı: Genellikle evlerde tuvalet ve lavabo temizliğinde kullanılan çok güçlü bir temizlik malzemesidir.
- Formülü: HNO₃
- Sistematik Adı: Nitrik asit
- Piyasa Adı:Kezzap
- Kullanım Alanı: Çok kuvvetli bir asittir. Gübre yapımında ve patlayıcı olan dinamitin üretiminde kullanılır.
- Formülü: H₂SO₄
- Sistematik Adı: Sülfürik asit
- Piyasa Adı:Zaç yağı
- Kullanım Alanı: Sanayide çok önemli bir maddedir. Gübre ve boya üretiminde sıkça kullanılır. Arabaların akülerinde de bu asit bulunur.
BAZLAR
- Formülü: NaOH
- Sistematik Adı: Sodyum hidroksit
- Piyasa Adı:Sud-kostik
- Kullanım Alanı: Lavabo açıcı olarak da bilinen bu madde; sabun, kâğıt, boya ve deterjan yapımında kullanılır.
- Formülü: KOH
- Sistematik Adı: Potasyum hidroksit
- Piyasa Adı:Potas-kostik
- Kullanım Alanı: Arap sabunu olarak bilinen yumuşak sabunların yapımında, pillerde ve gübre üretiminde kullanılır.
- Formülü: Ca(OH)₂
- Sistematik Adı: Kalsiyum hidroksit
- Piyasa Adı:Sönmüş kireç
- Kullanım Alanı: İnşaatlarda harç ve sıva yapımında, ayrıca çimento üretiminde kullanılır.
- Formülü: NH₃
- Sistematik Adı: Amonyak
- Piyasa Adı:Amonyak
- Kullanım Alanı: Keskin bir kokusu vardır. Temizlik malzemelerinde, gübre üretiminde ve hatta saç boyalarında bile kullanılır.
Soru 2: “Asit mi Baz mı?” etkinliği nasıl yapılır ve bu etkinlikten ne öğrenmemiz beklenir?
Bu etkinlik, laboratuvarda kullandığımız turnusol kâğıdı gibi ayıraçların yerine, evde bulabileceğimiz doğal malzemelerle nasıl kendi ayracımızı yapabileceğimizi gösteriyor. Çok eğlenceli ve öğretici bir deneydir!
Çözüm:
Etkinliğin amacı, kırmızı lahana suyunu kullanarak çeşitli maddelerin asit mi yoksa baz mı olduğunu anlamaktır. Kırmızı lahana suyu, doğal bir indikatör (belirteç veya ayıraç) görevi görür.
Adım 1: Doğal Ayıracımızı Hazırlayalım
Önce kırmızı lahanayı küçük küçük doğrayıp bir tencereye koyuyoruz. Üzerini geçecek kadar sıcak su ekleyip 7-8 dakika bekletiyoruz. Su, lahananın içindeki renk veren maddeyi (antosiyanin) çözecektir. Sonra soğumasını bekleyip bu mor renkli suyu bir süzgeç yardımıyla bir bardağa veya behere süzüyoruz. İşte mor renkli lahana suyumuz artık hazır! Bu bizim doğal asit-baz ayracımız.
Adım 2: Maddeleri Test Edelim ve Sonuçları Yorumlayalım
Kitapta deneyin devamı anlatılmamış ama amaç kısmından ne yapacağımızı anlıyoruz. Hazırladığımız lahana suyundan farklı bardaklara bir miktar koyup, üzerine test edeceğimiz maddeleri (limon suyu, sirke, sabunlu su, deterjan, çamaşır suyu, süt, karbonatlı su vb.) damlatacağız. Gözlemleyeceğimiz renk değişimleri bize o maddenin asit mi yoksa baz mı olduğunu söyleyecek.
Peki ne görmeyi bekliyoruz?
Temel Kural: Kırmızı lahana suyu asitlerle temas ettiğinde kırmızı ve pembe tonlarına, bazlarla temas ettiğinde ise mavi, yeşil, hatta sarı tonlarına döner. Nötr maddelerde ise kendi mor rengini korur.
Beklenen Sonuçlar:
- Lahana suyuna limon suyu veya sirke (asit) damlatırsan, sıvının rengi anında pembeye veya kırmızıya döner.
- Lahana suyuna sabunlu su, deterjanlı su veya karbonatlı su (baz) damlatırsan, sıvının rengi maviye veya yeşile döner.
- Lahana suyuna çok kuvvetli bir baz olan çamaşır suyu eklersen, renk sarıya bile dönebilir.
- Lahana suyuna saf su veya süt (nötre yakın) eklersen, renginde belirgin bir değişiklik olmaz, mor kalır veya çok hafif bir renk değişimi olur.
Kısacası bu etkinlik sayesinde, bir maddenin kimliğini, onda meydana getirdiği renk değişimine bakarak nasıl tespit edebileceğimizi öğreniyoruz. Doğanın bize ne kadar harika laboratuvar malzemeleri sunduğunu da görmüş oluyoruz!
Umarım açıklamalarım faydalı olmuştur. Başarılar dilerim!
