Harika bir çalışma! Merhaba sevgili öğrencilerim, ben Fen Bilimleri öğretmeniniz. Şimdi bu “Neler Öğrendik?” bölümündeki soruları hep birlikte, adım adım ve anlayarak çözeceğiz. Unutmayın, Fen Bilimleri mantık ve gözlemle çok daha kolay hale gelir. Hadi başlayalım!
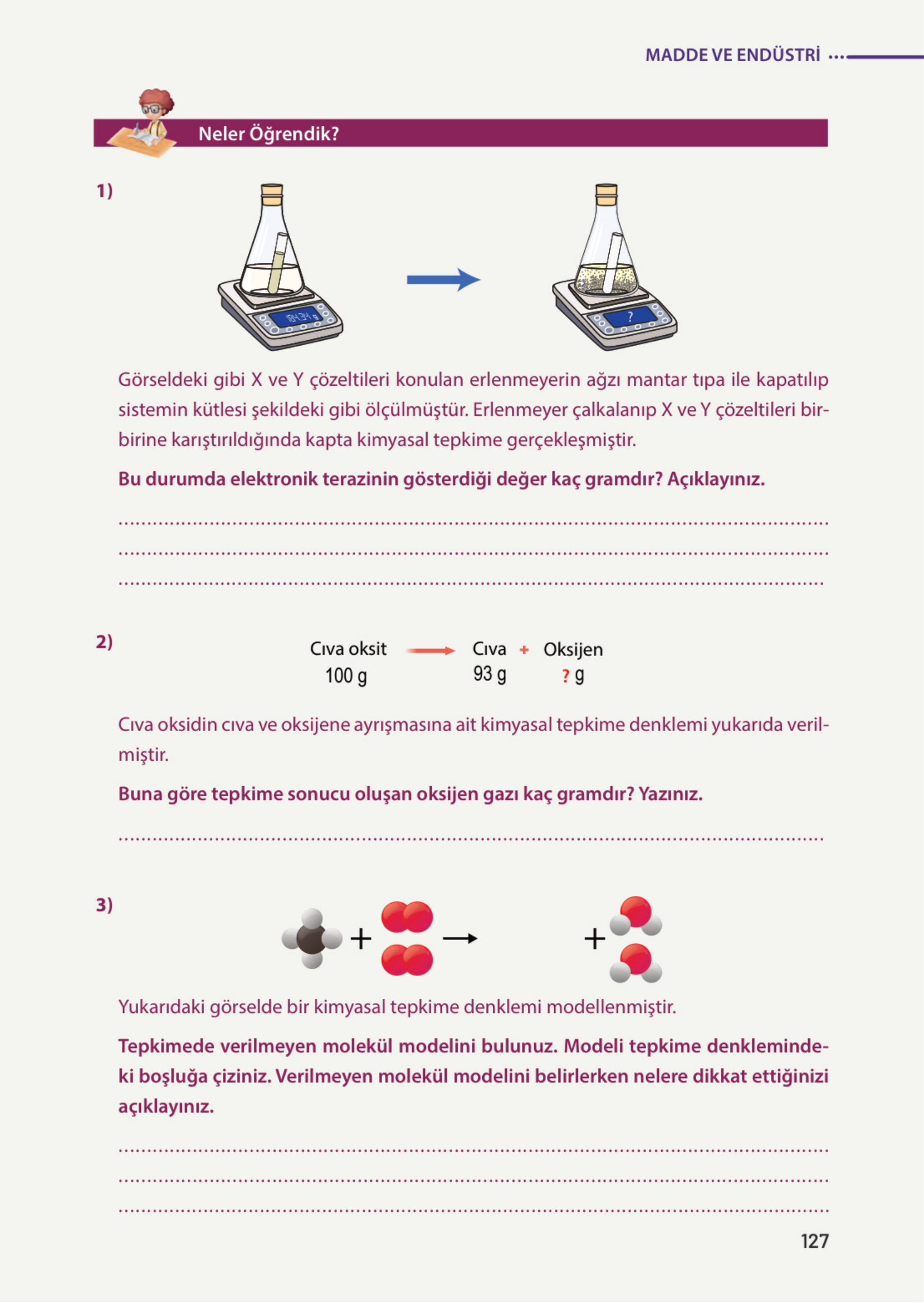
1) Görseldeki gibi X ve Y çözeltileri konulan erlenmeyerin ağzı mantar tıpa ile kapatılıp sistemin kütlesi şekildeki gibi ölçülmüştür. Erlenmeyer çalkalanıp X ve Y çözeltileri birbirine karıştırıldığında kapta kimyasal tepkime gerçekleşmiştir. Bu durumda elektronik terazinin gösterdiği değer kaç gramdır? Açıklayınız.
Merhaba çocuklar, bu soru aslında kimyasal tepkimelerin en temel kurallarından birini içeriyor. Hadi adım adım gidelim.
Unutma: Kimyasal tepkimelerde kütle her zaman korunur! Buna Kütlenin Korunumu Kanunu diyoruz. Yani, tepkimeye giren maddelerin toplam kütlesi, tepkime sonunda oluşan ürünlerin toplam kütlesine her zaman eşittir.
Adım 1: Soruya bakalım. Elimizde bir erlenmeyer (cam kap), içinde X ve Y çözeltileri var. Bu kabın ağzı ne ile kapatılmış? Evet, bir mantar tıpa ile! Bu çok önemli bir detay. Kabın ağzının kapalı olması, tepkime sırasında herhangi bir gaz çıkışı olsa bile, bu gazın dışarı kaçmasını engeller. Yani sistemimiz kapalı bir sistem.
Adım 2: Tepkime başlamadan önce terazi kaç gramı gösteriyor? Görsele baktığımızda 184,34 g olduğunu görüyoruz. Bu bizim başlangıçtaki toplam kütlemizdir. (Erlenmeyer + Tıpa + X çözeltisi + Y çözeltisi = 184,34 g)
Adım 3: Kap çalkalanıyor ve X ile Y maddeleri arasında bir kimyasal tepkime gerçekleşiyor. Kütlenin Korunumu Kanunu’na göre, kapalı kaplarda gerçekleşen kimyasal tepkimelerde kütle değişmez. Atomlar sadece yeniden düzenlenerek yeni maddeler oluşturur, yok olmazlar veya yeniden var olmazlar.
Sonuç:
Bu nedenle, tepkime bittikten sonra da terazinin göstereceği değer başlangıçtaki değerle aynı olacaktır.
Terazinin göstereceği değer 184,34 gramdır.
2) Civa oksidin cıva ve oksijene ayrışmasına ait kimyasal tepkime denklemi yukarıda verilmiştir. Buna göre tepkime sonucu oluşan oksijen gazı kaç gramdır? Yazınız.
Bu soruda da yine Kütlenin Korunumu Kanunu’nu kullanacağız. Bu kanunun ne kadar önemli olduğunu görüyorsunuz değil mi?
Tepkime denklemimiz şu şekilde:
Civa oksit ⟶ Civa + Oksijen
Okun sol tarafındaki maddelere girenler, sağ tarafındakilere ise ürünler diyoruz. Kuralımız neydi?
Girenlerin Toplam Kütlesi = Ürünlerin Toplam Kütlesi
Adım 1: Bize verilen değerleri bu denkleme yerleştirelim.
- Girenler: 100 g Civa oksit
- Ürünler: 93 g Civa + ? g Oksijen
Adım 2: Şimdi bu değerleri formülümüze yazalım.
100 g = 93 g + ? g
Adım 3: Oksijenin kütlesini bulmak için basit bir çıkarma işlemi yapmamız gerekiyor. Toplam ürün kütlesinden (100 g), bildiğimiz cıva kütlesini (93 g) çıkaracağız.
Oksijenin Kütlesi = 100 g – 93 g
Sonuç:
Oluşan oksijen gazı 7 gramdır.
3) Yukarıdaki görselde bir kimyasal tepkime denklemi modellenmiştir. Tepkimede verilmeyen molekül modelini bulunuz. Modeli tepkime denklemindeki boşluğa çiziniz. Verilmeyen molekül modelini belirlerken nelere dikkat ettiğinizi açıklayınız.
Bu soru da bir önceki soru gibi ama bu sefer gramlar yerine atomları sayacağız. Çünkü kimyasal tepkimelerde kütle korunduğu gibi, atom sayısı ve cinsi de korunur. Yani girenlerde ne kadar ve hangi tür atom varsa, ürünlerde de o kadar ve o tür atom olmalıdır!
Hadi atom sayımı yapalım!
Adım 1: Girenlerdeki (okun sol tarafı) atomları sayalım.
- Siyah atomdan: 1 tane
- Beyaz atomdan: 4 tane
- Kırmızı atomdan: İki molekülde toplam 2 + 2 = 4 tane
Yani tepkimeye 1 siyah, 4 beyaz ve 4 kırmızı atom girmiş.
Adım 2: Ürünlerdeki (okun sağ tarafı) bilinen atomları sayalım.
- İki tane su molekülü görüyoruz. Her birinde 1 kırmızı ve 2 beyaz atom var.
- Kırmızı atomdan: 1 + 1 = 2 tane
- Beyaz atomdan: 2 + 2 = 4 tane
- Siyah atomdan: 0 tane
Adım 3: Eksik atomları bulalım.
Şimdi girenler ve ürünler arasındaki farka bakalım.
- Siyah atom: Girenlerde 1 tane vardı, ürünlerde 0 tane var. Demek ki eksik molekülde 1 tane siyah atom olmalı.
- Beyaz atom: Girenlerde 4 tane vardı, ürünlerde 4 tane var. Eksik yok.
- Kırmızı atom: Girenlerde 4 tane vardı, ürünlerde 2 tane var. Demek ki eksik molekülde 4 – 2 = 2 tane kırmızı atom olmalı.
Sonuç:
Bulmamız gereken molekül; 1 tane siyah atom ve ona bağlı 2 tane kırmızı atomdan oluşmalıdır. Bu molekül, ortada bir siyah atom ve iki yanında birer kırmızı atom olacak şekilde çizilmelidir. (Bu molekül aslında karbondioksit (CO₂) molekülüdür.)
Açıklama: Verilmeyen molekülü belirlerken, kimyasal tepkimelerde atom cinsi ve sayısının korunduğu ilkesine dikkat ettim. Tepkimeye giren atomların sayısını ve türünü belirledikten sonra, tepkime sonucu oluşan ürünlerdeki atomların sayısını ve türünü saydım. Aradaki fark, verilmeyen molekülü oluşturan atomları verdi.
