Merhaba sevgili öğrencilerim! Ben Fen Bilimleri öğretmeniniz. Bugün kitabımızdaki “Bileşiklerin Formülleri, İsimleri ve Bazı Kullanım Alanları” konusunu birlikte inceleyeceğiz. Bana gönderdiğiniz görseldeki bilgileri, sanki sınıftaymışız gibi adım adım, sorularla ve cevaplarla ele alalım. Hazırsanız, başlayalım!
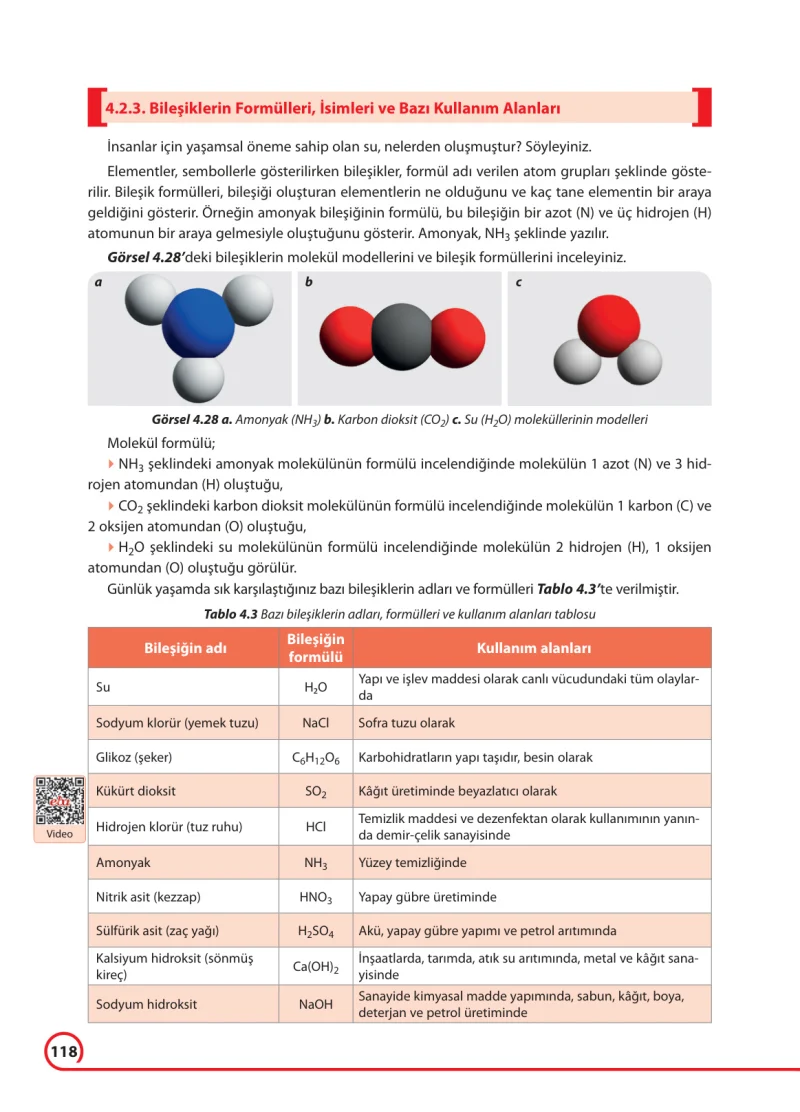
Soru 1: Görsel 4.28’de verilen amonyak (a), karbondioksit (b) ve su (c) moleküllerinin modelleri bize ne anlatıyor?
Bu modeller, atomların bir araya gelerek molekülleri nasıl oluşturduğunu gösteren minik maketler gibidir. Her bir renkli top farklı bir elementin atomunu temsil eder. Gelin bu modelleri tek tek inceleyelim.
Adım 1: Amonyak (NH₃) Modeli (Görsel a)
Görsel ‘a’ amonyak molekülünü gösteriyor. Bu modelde ortada büyük, mavi bir top ve ona bağlı üç tane daha küçük, beyaz top görüyoruz. Bu şu anlama geliyor:
- Ortadaki büyük mavi top, bir tane Azot (N) atomunu temsil eder.
- Etrafındaki üç beyaz top ise üç tane Hidrojen (H) atomunu temsil eder.
Sonuç olarak, bir amonyak molekülü 1 Azot ve 3 Hidrojen atomunun birleşmesiyle oluşur. Formülü de bu yüzden NH₃‘tür.
Adım 2: Karbondioksit (CO₂) Modeli (Görsel b)
Görsel ‘b’ ise soluk alıp verdiğimizde dışarı üflediğimiz karbondioksit molekülünü gösteriyor. Bu modelde de ortada siyah bir top ve iki yanında kırmızı toplar var.
- Ortadaki siyah top, bir tane Karbon (C) atomunu temsil eder.
- İki yanındaki kırmızı toplar ise iki tane Oksijen (O) atomunu temsil eder.
Yani bir karbondioksit molekülü, 1 Karbon ve 2 Oksijen atomundan oluşur. Bu yüzden formülü CO₂ olarak yazılır.
Adım 3: Su (H₂O) Modeli (Görsel c)
Görsel ‘c’ hayatımızın vazgeçilmezi olan su molekülünü gösteriyor. Burada da büyük kırmızı bir top ve ona bağlı iki küçük beyaz top var. Tıpkı bir çizgi film karakterinin kafasına benziyor, değil mi?
- Büyük kırmızı top, bir tane Oksijen (O) atomunu temsil eder.
- Ona bağlı iki beyaz top ise iki tane Hidrojen (H) atomunu temsil eder.
Demek ki bir su molekülü, 2 Hidrojen ve 1 Oksijen atomundan meydana gelir. Formülü de bu yüzden H₂O‘dur.
Soru 2: Tablo 4.3’te verilen bazı önemli bileşikler ve kullanım alanları nelerdir? Bu tablodan ne öğrenmeliyiz?
Bu tablo, günlük hayatta sıkça karşılaştığımız veya adını duyduğumuz bazı bileşiklerin kimlik kartı gibidir. Bize hem formülünü hem de nerelerde kullanıldığını özetler. Gelin tablodaki birkaç önemli örneği birlikte inceleyelim.
Bileşiğin Adı: Sodyum klorür (Yemek Tuzu)
Formülü: NaCl
Açıklama: Sofralarımızın vazgeçilmezi olan tuzun formülüdür. Bir tane Sodyum (Na) ve bir tane Klor (Cl) atomundan oluşur. En bilinen kullanımı sofra tuzu olmasıdır.
Bileşiğin Adı: Glikoz (Şeker)
Formülü: C₆H₁₂O₆
Açıklama: Vücudumuzun temel enerji kaynağı olan basit şekerin formülüdür. Bakın ne kadar çok atomdan oluşuyor! 6 Karbon, 12 Hidrojen ve 6 Oksijen atomu içerir. Karbonhidratların yapı taşıdır ve besin olarak kullanılır.
Bileşiğin Adı: Hidrojen klorür (Tuz Ruhu)
Formülü: HCl
Açıklama: Evlerde temizlik malzemesi olarak, özellikle kireç ve pas sökücü olarak kullanılan çok kuvvetli bir asittir. Bir Hidrojen (H) ve bir Klor (Cl) atomundan oluşur. Sanayide de kullanılır.
Bileşiğin Adı: Sülfürik asit (Zaç Yağı)
Formülü: H₂SO₄
Açıklama: Arabaların akülerinde bulunan asit budur. Çok güçlü bir maddedir ve sanayide gübre yapımı, petrol arıtımı gibi birçok alanda kullanılır. Formülüne baktığımızda 2 Hidrojen (H), 1 Kükürt (S) ve 4 Oksijen (O) atomu içerdiğini görürüz.
Bileşiğin Adı: Kalsiyum hidroksit (Sönmüş Kireç)
Formülü: Ca(OH)₂
Açıklama: İnşaatlarda harç yapımında, tarımda toprağın asitliğini düzenlemek için ve atık suların temizlenmesinde kullanılır. Formüldeki parantez ve ‘2’ sayısı, parantez içindeki OH grubundan iki tane olduğunu gösterir. Yani 1 Kalsiyum (Ca), 2 Oksijen (O) ve 2 Hidrojen (H) atomu vardır.
Umarım bu açıklamalar konuyu daha iyi anlamanıza yardımcı olmuştur. Gördüğünüz gibi, kimya dersinde öğrendiğimiz formüller aslında etrafımızdaki her şeyin yapı taşlarını anlatıyor. Anlamadığınız bir yer olursa çekinmeden tekrar sorun. Başarılar dilerim!
